01/09/2012
El dolor persistente, especialmente aquel asociado con la inflamación, es una condición desafiante que afecta a millones de personas. En la búsqueda de tratamientos efectivos, la Electroacupuntura (EA) ha surgido como una modalidad terapéutica prometedora. A diferencia de la acupuntura manual, la EA utiliza una corriente eléctrica suave aplicada a través de las agujas, intensificando la estimulación. Pero, ¿funciona realmente y, lo que es más importante, cómo?
La investigación científica ha profundizado en los efectos y mecanismos de la acupuntura y la electroacupuntura en el dolor persistente, utilizando modelos animales de dolor inflamatorio, a menudo inducidos con sustancias como el adyuvante completo de Freund (CFA) o la carragenina. Estos estudios han explorado la acción de la EA en múltiples niveles del sistema nervioso: periférico, espinal y supraespinal.
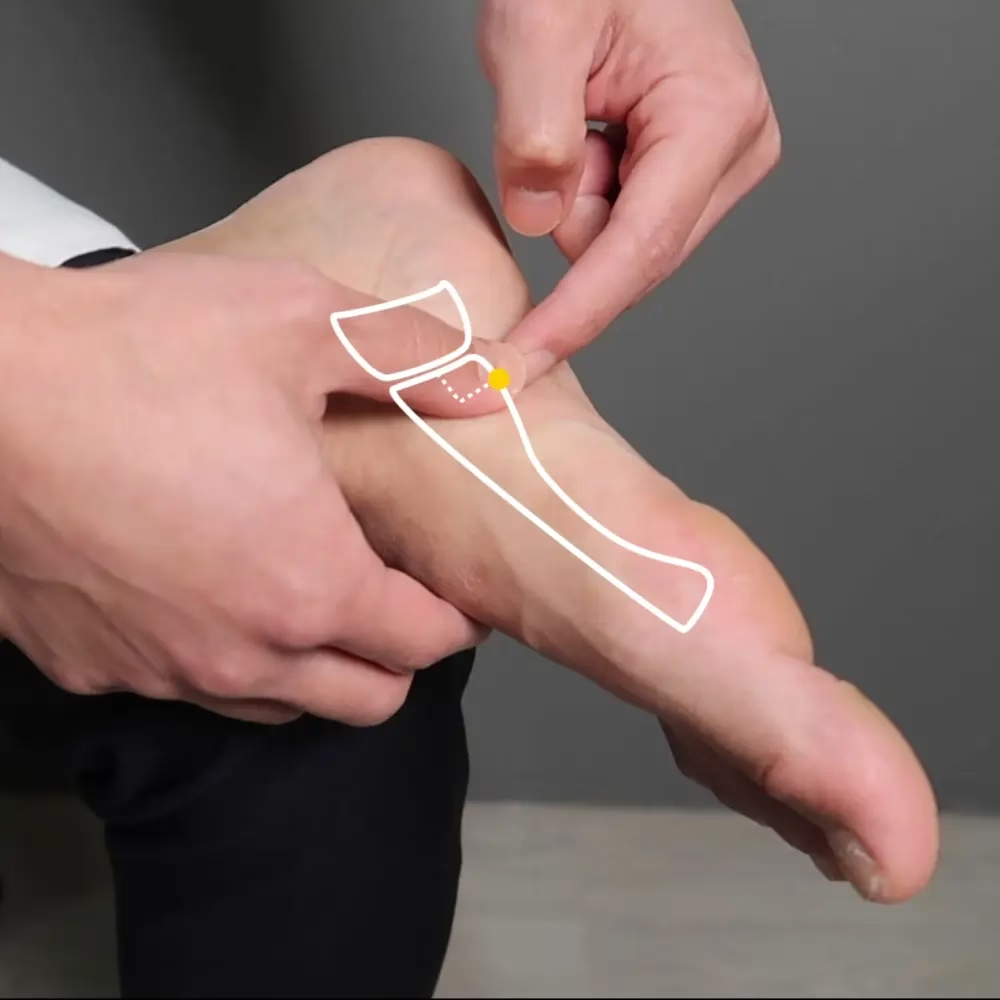
Aunque la compleja red de interacciones aún se está desentrañando, la evidencia actual sugiere firmemente que la EA induce efectos analgésicos significativos a través de la modulación de diversas sustancias bioactivas y vías de señalización. Comprender estos mecanismos es clave para validar y optimizar el uso de la electroacupuntura en el manejo del dolor.
Mecanismos Periféricos de la Electroacupuntura en el Dolor Inflamatorio
A nivel de los tejidos inflamados, la electroacupuntura ejerce efectos analgésicos al influir en el entorno bioquímico local. Uno de los hallazgos más consistentes es su capacidad para aumentar los niveles de opioides endógenos en los sitios de inflamación. Esto ocurre a través de al menos dos vías principales.
Primero, la EA puede activar las fibras nerviosas simpáticas. Esta activación simpática parece mejorar la migración de células que contienen opioides, como los leucocitos polimorfonucleares y las células mononucleares, hacia el sitio lesionado. Una vez allí, estas células pueden liberar sus reservas de opioides.
Segundo, la EA estimula el eje hipotálamo-hipófisis-suprarrenal (HPA), lo que lleva a una disminución de la enzima COX-2 (ciclooxigenasa-2). La reducción de COX-2 interfiere con el metabolismo de los endocannabinoides, lo que a su vez conduce a un aumento de los niveles de opioides en el sitio de la lesión. Además, la disminución de COX-2 por sí sola puede reducir los niveles de prostaglandina E2 (PGE2), una sustancia conocida por sensibilizar los nociceptores periféricos y contribuir al dolor.
Los endocannabinoides, como la anandamida, también juegan un papel. La EA puede aumentar los niveles de endocannabinoides, y se ha demostrado que la activación del receptor CB2 (CB2R) por estos compuestos inhibe directamente la actividad de los nervios sensoriales en modelos de dolor. La EA también parece aumentar la expresión de receptores CB2 (CB2R) en células inmunes y queratinocitos en el tejido inflamado, lo que potencia aún más la señalización de los endocannabinoides y la subsiguiente upregulation de opioides.
Otras sustancias bioactivas periféricas también están implicadas. El factor liberador de corticotropina (CRF) y la adenosina son ejemplos. Se ha demostrado que un antagonista del CRF administrado localmente previene la inhibición del dolor inflamatorio por la EA. El CRF puede bloquear el dolor estimulando la liberación de opioides de las células inmunes. La adenosina, actuando sobre los receptores A1, también media los efectos analgésicos de la acupuntura y la electroacupuntura, suprimiendo la hipersensibilidad y las respuestas neuronales en el cerebro.
En conjunto, estos hallazgos subrayan que los opioides periféricos desempeñan un papel central en la inhibición del dolor inflamatorio por la electroacupuntura. Actúan bloqueando la liberación de citoquinas proinflamatorias por parte de las células inmunes y desensibilizando las terminaciones nerviosas sensoriales periféricas al interactuar con los receptores opioides locales.
Mecanismos Espinales de la Electroacupuntura
El dolor no solo se percibe a nivel periférico, sino que se transmite y modula en la médula espinal. La electroacupuntura influye significativamente en estos procesos espinales, atenuando la transmisión de señales nocivas.
Opioides Espinales y Frecuencia de Estimulación
La acción de la EA sobre los receptores opioides espinales varía dependiendo de si el dolor es agudo o persistente, y de la frecuencia de la estimulación. En modelos animales sin lesión previa (dolor agudo), la EA de baja frecuencia (2 Hz) activa vías que involucran endorfinas, endomorfinas y encefalinas, mientras que la EA de alta frecuencia (100 Hz) activa la dinorfina para suprimir el dolor.
Sin embargo, en condiciones de dolor persistente inflamatorio, la situación cambia. Tanto la EA de 10 Hz como la de 100 Hz pueden inhibir el dolor, pero sus efectos pueden diferir en duración. En modelos de dolor inflamatorio, la inhibición del dolor por EA de 10 Hz y 100 Hz es bloqueada por antagonistas de los receptores opioides μ y δ administrados intratecalmente (en el espacio espinal), pero no por un antagonista del receptor κ. Esto sugiere un cambio en la participación de los subtipos de receptores opioides durante el dolor persistente, posiblemente debido a cambios en su sensibilidad.
La siguiente tabla resume la participación diferencial de los receptores opioides según el modelo de dolor y la frecuencia de la EA:
| Modelo | Frecuencia EA | Prueba | Receptores Opioides Implicados |
|---|---|---|---|
| Sin lesión | 2 Hz | Reflejo de la cola (Tail flick) | μ |
| Sin lesión | 15 Hz | Reflejo de la cola | μ, δ, y κ |
| Sin lesión | 100 Hz | Reflejo de la cola | κ |
| Esguince de tobillo | 2Hz/100 Hz (trenes) | Fuerza al caminar | Ninguno (inyección sistémica) |
| Esguince de tobillo | 10 Hz | Fuerza al caminar | Ninguno (inyección sistémica) |
| CFA intra-plantar | 10 Hz y 100 Hz | Latencia de retirada de la pata | μ y δ |
| Capsaicina intra-plantar | 2Hz/100 Hz (trenes) | Umbral mecánico | μ y δ |
| Carragenina intra-rodilla | 10 Hz | Fuerza de soporte de peso | μ |
| Neuropatía por quimioterapia | 10 Hz | Umbral mecánico | μ, δ, y κ |
La implicación de los receptores opioides μ y δ en el dolor persistente es clínicamente relevante. Sugiere que la EA podría potenciar el efecto de los analgésicos opioides convencionales, permitiendo quizás la reducción de dosis y minimizando los efectos secundarios. Estudios combinando EA y morfina a bajas dosis han mostrado un mejor control del dolor inflamatorio que cualquiera de las terapias por separado.
Además de los opioides clásicos, el sistema nociceptina/orphanina FQ (N/OFQ) y sus receptores tipo opioide también modulan el dolor. La EA puede aumentar los niveles de N/OFQ y sus receptores en la médula espinal en modelos de dolor inflamatorio, contribuyendo a la analgesia.
Por otro lado, la colecistoquinina octapéptido (CCK-8), un antagonista fisiológico de los opioides endógenos en el sistema nervioso central, puede atenuar la analgesia inducida por EA. La investigación sugiere que una función de CCK atenuada podría promover los efectos analgésicos de la acupuntura/EA y la morfina, abriendo la posibilidad de que los antagonistas de los receptores CCK puedan aumentar la sensibilidad a la acupuntura.
Norepinefrina y Serotonina
Los sistemas descendentes de control del dolor que involucran norepinefrina y serotonina (5-HT) son cruciales. La electroacupuntura puede activar neuronas en el tronco encefálico (núcleo del rafe magno, locus coeruleus) que proyectan a la médula espinal y liberan estos neurotransmisores. Numerosos estudios confirman la participación de la serotonina y la norepinefrina espinal en la analgesia por EA.
Antagonistas de receptores adrenérgicos (para norepinefrina) y serotoninérgicos (para serotonina) administrados sistémica o intratecalmente han demostrado bloquear o atenuar los efectos analgésicos de la EA en diversos modelos de dolor. Específicamente, los estudios intratecales apuntan a la participación de los receptores α2a-adrenérgicos y los receptores 5-HT1A y 5-HT2A en la médula espinal en la mediación de los efectos de la EA, dependiendo de la frecuencia de estimulación y el tipo de dolor.
Se cree que la norepinefrina espinal liberada por la EA actúa presinápticamente para disminuir la liberación de glutamato, un neurotransmisor excitatorio clave en la transmisión del dolor. La serotonina espinal, por su parte, podría actuar postsinápticamente para suprimir la fosforilación de subunidades de receptores de glutamato (como NMDA), reduciendo así la excitabilidad neuronal asociada al dolor.
La interacción entre opioides, serotonina y norepinefrina espinal en la acción de la EA es compleja y probablemente sinérgica. Clínicamente, esto es relevante, ya que los inhibidores de la recaptación de serotonina y norepinefrina (IRSN) y los inhibidores selectivos de la recaptación de serotonina (ISRS) se utilizan para el manejo del dolor crónico. La EA, al aumentar la liberación de estos neurotransmisores, podría potenciar los efectos de estos medicamentos, permitiendo potencialmente reducir sus dosis.
Glutamato y sus Receptores
El glutamato y sus receptores (NMDA, AMPA, kainato, metabotrópicos) son abundantes en el asta dorsal de la médula espinal y son fundamentales en la transmisión de señales nocivas. En modelos de dolor inflamatorio, la EA a diferentes frecuencias (2, 15, 120 Hz) no solo alivia el dolor, sino que también disminuye la expresión o la fosforilación (activación) de subunidades de receptores de glutamato como GluN1, GluN2A y GluA1 en el asta dorsal y los ganglios de la raíz dorsal (DRG).
Esto sugiere que la EA inhibe la transmisión de mensajes nocivos a nivel espinal al amortiguar la actividad de los receptores de glutamato. Como se mencionó, esto podría lograrse indirectamente a través del aumento de norepinefrina, serotonina y opioides espinales, que pueden modular la función de los receptores NMDA.
La combinación de EA con antagonistas de los receptores NMDA a bajas dosis ha demostrado ser más efectiva que cualquiera de las terapias por separado en modelos de dolor inflamatorio. Esto refuerza la idea de que la EA actúa, al menos en parte, modulando la vía del glutamato, y sugiere un potencial sinergismo entre la EA y los medicamentos que actúan sobre los receptores NMDA.
Células Gliales y Citoquinas
Las células gliales (astrocitos y microglía) en la médula espinal se activan en respuesta a la inflamación y la lesión nerviosa, liberando citoquinas proinflamatorias (IL-1β, IL-6, TNF-α) que amplifican las señales de dolor. La electroacupuntura ha demostrado inhibir la activación de estas células gliales y disminuir los niveles de citoquinas proinflamatorias en la médula espinal en modelos de dolor inflamatorio.
Al reducir las citoquinas proinflamatorias, la EA interrumpe un ciclo que perpetúa el dolor. Por ejemplo, se sabe que la IL-1β aumenta la fosforilación de GluN1, facilitando el dolor, y que el TNF-α aumenta las corrientes NMDA. Al suprimir estas citoquinas, la EA reduce la hiperexcitabilidad espinal.
La inhibición de la activación glial y la producción de citoquinas por la EA podría estar mediada por la liberación de opioides y N/OFQ espinales. Los opioides pueden bloquear la liberación de Sustancia P (SP), un neuropéptido que activa las células gliales. El N/OFQ también ha demostrado suprimir la expresión génica de citoquinas en astrocitos.
Moléculas de Señalización
La EA también influye en cascadas de señalización intracelular dentro de las neuronas y células gliales espinales. En modelos de dolor inflamatorio, la EA puede disminuir la fosforilación de proteínas como Akt y p38 MAPK, que están implicadas en la iniciación y mantenimiento de la hipersensibilidad inflamatoria y la transmisión del dolor.
La activación de receptores opioides μ y δ puede inhibir la liberación de Sustancia P, lo que a su vez reduce la fosforilación de Akt. De manera similar, la inhibición de citoquinas proinflamatorias y la modulación de receptores (como los receptores de neurokinina-1) por la EA pueden conducir a la supresión de la vía p38 MAPK/ATF-2, atenuando el dolor.
Estos hallazgos a nivel molecular complementan los mecanismos neuroquímicos, mostrando que la EA actúa en cascadas de señalización intracelular que son críticas para la procesamiento del dolor en la médula espinal.
Implicaciones Clínicas y Futuras Direcciones
La comprensión de estos complejos mecanismos periféricos y espinales de la electroacupuntura tiene importantes implicaciones clínicas. La evidencia de que la EA aumenta los opioides endógenos, modula neurotransmisores como serotonina y norepinefrina, e influye en el sistema glutamatérgico y las citoquinas gliales, sugiere que la EA podría ser una terapia adyuvante valiosa para el manejo del dolor.
La posibilidad de combinar la EA con medicamentos como opioides, IRSN/ISRS o antagonistas de NMDA para lograr un mejor control del dolor con dosis más bajas de fármacos es particularmente interesante y respaldada por algunos hallazgos de investigación.
A pesar de los avances, aún quedan áreas por investigar. La participación de otras sustancias bioactivas como la bradicinina, el factor de crecimiento nervioso y los canales de potencial receptor transitorio en la analgesia por EA necesita ser explorada. La modulación de la síntesis de CRF y adenosina por la EA también requiere más estudio. Además, la aplicación directa de estos hallazgos en ensayos clínicos en humanos es fundamental para confirmar su relevancia clínica.
Preguntas Frecuentes sobre la Electroacupuntura y el Dolor
- ¿Es la electroacupuntura diferente de la acupuntura tradicional para el dolor? Sí, la electroacupuntura utiliza una corriente eléctrica suave aplicada a través de las agujas de acupuntura, lo que proporciona una estimulación continua y controlada. La investigación sugiere que esta estimulación eléctrica puede potenciar ciertos mecanismos analgésicos en comparación con la manipulación manual de las agujas.
- ¿Cómo ayuda la electroacupuntura con el dolor inflamatorio? La electroacupuntura actúa a varios niveles. A nivel periférico, aumenta los opioides naturales en el sitio inflamado y reduce sustancias que causan dolor como la PGE2. A nivel espinal, modula la actividad de las neuronas del dolor a través de opioides, serotonina, norepinefrina, glutamato y reduciendo la inflamación glial.
- ¿La frecuencia de la electroacupuntura importa? Sí, la investigación sugiere que diferentes frecuencias (como 2 Hz vs. 100 Hz) pueden activar distintos mecanismos y vías de opioides espinales, y pueden tener efectos diferentes en el dolor agudo versus persistente.
- ¿Puede la electroacupuntura ayudar a reducir la necesidad de analgésicos? Los estudios preclínicos sugieren que la electroacupuntura, al potenciar las vías analgésicas endógenas y modular la transmisión del dolor, podría permitir el uso de dosis más bajas de medicamentos analgésicos, como opioides o ciertos antidepresivos.
- ¿Se conocen todos los mecanismos de la electroacupuntura? Aunque se han identificado muchos mecanismos importantes que involucran opioides, neurotransmisores, citoquinas y vías de señalización, la investigación continúa explorando otras sustancias y vías implicadas para comprender completamente cómo la electroacupuntura alivia el dolor.
Conclusión
La investigación, particularmente en modelos preclínicos de dolor inflamatorio, proporciona una base científica sólida para la efectividad de la electroacupuntura en el manejo del dolor persistente. Los estudios han revelado una intrincada red de mecanismos que operan a nivel periférico y espinal, incluyendo la liberación de opioides endógenos, la modulación de sistemas de neurotransmisores como la serotonina y la norepinefrina, la influencia sobre el glutamato y sus receptores, y la supresión de la inflamación mediada por células gliales. Estos hallazgos no solo validan el uso de la electroacupuntura, sino que también abren la puerta a estrategias de manejo del dolor más integrales, combinando la EA con terapias farmacológicas convencionales para potenciar los efectos y optimizar los resultados para los pacientes que sufren de dolor crónico.
Si quieres conocer otros artículos parecidos a Electroacupuntura y Dolor: ¿Funciona? puedes visitar la categoría Acupuntura.


Conoce mas Tipos