18/05/2017
Nuestro intestino se enfrenta diariamente a un desafío monumental: procesar los alimentos que ingerimos mientras convive con billones de bacterias y se defiende de potenciales patógenos. En este campo de batalla y coexistencia, un sistema especializado trabaja incansablemente para mantener el equilibrio: el tejido linfoide asociado al intestino, conocido como GALT por sus siglas en inglés (Gut-Associated Lymphoid Tissue).
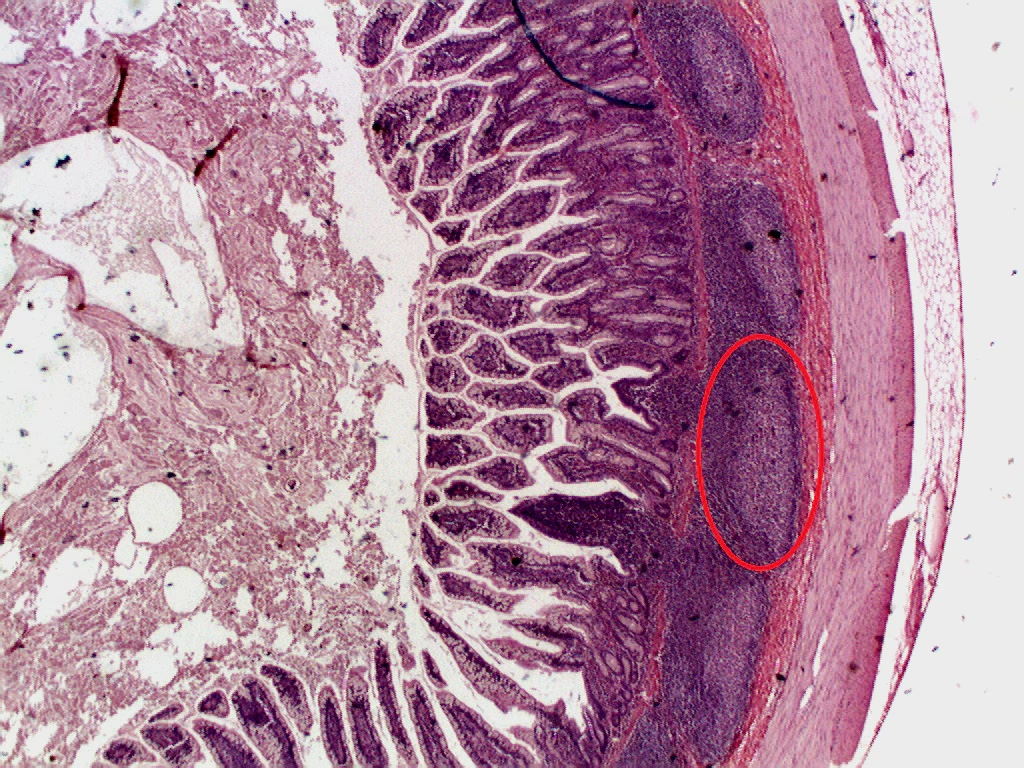
El GALT no es solo una pequeña parte del sistema inmunitario; de hecho, constituye su componente más extenso y complejo. Su ubicación estratégica, recubriendo gran parte del tracto gastrointestinal, le permite interactuar directamente con el contenido luminal, actuando como la primera y más crucial línea de defensa inmunitaria a nivel mucosal.
- ¿Qué es Exactamente el GALT?
- Anatomía y Estructura: Dos Compartimentos Clave
- Captación de Antígenos: La Puerta de Entrada
- Inducción de la Respuesta Inmune en el GALT Organizado
- Los Anticuerpos Mucosales: IgA, la Estrella Defensiva
- Características Únicas del GALT Moldeadas por la Microbiota
- Tabla Comparativa: Componentes del GALT
- Preguntas Frecuentes sobre el GALT
- Conclusión
¿Qué es Exactamente el GALT?
El GALT es una red compleja de células y estructuras linfoides dispersas a lo largo del tracto gastrointestinal. Su función primordial es monitorear constantemente el ambiente intestinal, identificando y respondiendo a las amenazas (patógenos) mientras, de forma igualmente vital, tolera las sustancias inocuas (componentes de la dieta y la microbiota intestinal comensal).
Esta dualidad de respuesta –ataque al peligro y tolerancia a lo inofensivo– es fundamental para nuestra salud. Una respuesta inmune exagerada contra los alimentos podría llevar a alergias, mientras que un ataque contra la microbiota podría alterar el equilibrio intestinal crucial. Por otro lado, una tolerancia excesiva permitiría la entrada de patógenos. El GALT domina este delicado balance.
Anatomía y Estructura: Dos Compartimentos Clave
Para cumplir su compleja misión, el GALT posee una organización anatómica distintiva que se divide en dos grandes compartimentos funcionales:
- GALT Organizado: Es la parte inductora de la respuesta inmunitaria. Aquí se inicia el reconocimiento antigénico y la activación de las células inmunes vírgenes. Está compuesto principalmente por:
- Placas de Peyer: Agregados linfoides macroscópicos, predominantemente en el íleon terminal. Son centros neurálgicos para la captación de antígenos luminales.
- Ganglios Linfáticos Mesentéricos: Situados en el mesenterio, reciben linfa del intestino y son otro sitio crucial para la interacción entre células presentadoras de antígeno (APC) y linfocitos.
- Folículos Linfoides Aislados: Estructuras más pequeñas y dispersas a lo largo del intestino.
- GALT Difuso: Es la parte efectora de la respuesta inmunitaria. Contiene poblaciones de células inmunes listas para actuar o ya activadas, dispersas en la mucosa intestinal. Incluye:
- Linfocitos Intraepiteliales (IEL): Residen entre las células epiteliales que forman la barrera intestinal. Son una población abundante y heterogénea, muchos con fenotipo citotóxico o supresor atípico. Proporcionan una respuesta rápida, especialmente contra células epiteliales infectadas, y juegan un papel importante en la tolerancia oral.
- Linfocitos de Lámina Propia (LPL): Se encuentran en la capa de tejido conectivo debajo del epitelio. Esta población incluye linfocitos T (principalmente colaboradores o Th), linfocitos B maduros que se diferencian en células plasmáticas productoras de anticuerpos, macrófagos, células dendríticas y mastocitos.
Captación de Antígenos: La Puerta de Entrada
La exposición constante a una enorme carga antigénica requiere mecanismos eficientes para muestrear el contenido luminal. Los antígenos pueden acceder al GALT por varias vías:
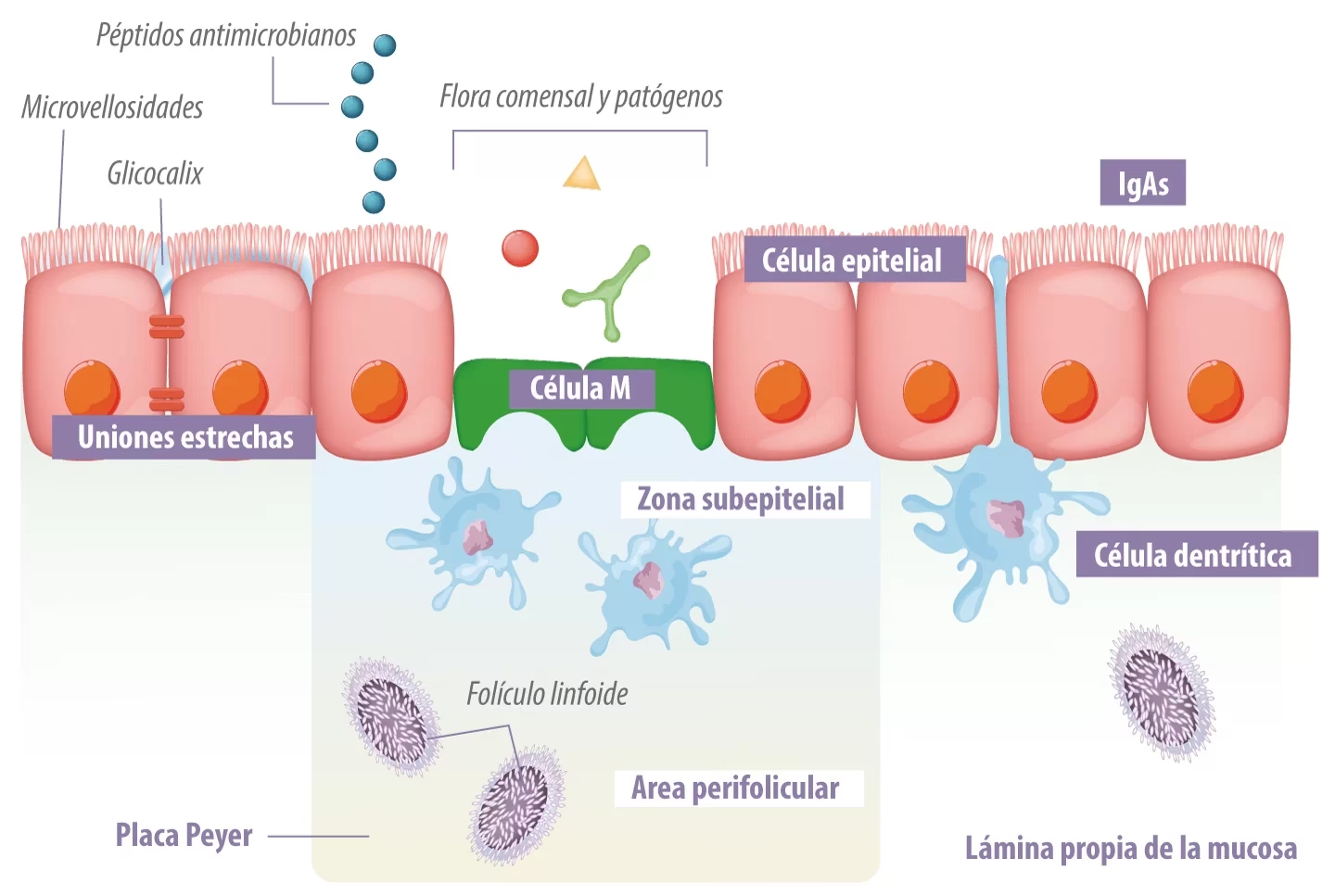
- Células M: Son enterocitos especializados en las Placas de Peyer y folículos aislados. Carecen de microvilli y glicocálix en su superficie luminal, lo que facilita la adhesión y captación de macromoléculas, partículas, virus y bacterias. Transportan estos antígenos mediante transcitosis a través de su citoplasma y los liberan en un "bolsillo" basolateral que alberga células inmunes, como células dendríticas y macrófagos, listas para procesarlos.
- Enterocitos: Aunque menos accesibles que las células M debido a su glicocálix, los enterocitos también pueden captar antígenos solubles, procesarlos y presentarlos a los linfocitos T.
- Vía Paracelular: Las células dendríticas pueden extender proyecciones a través de las uniones estrechas entre los enterocitos para muestrear antígenos directamente del lumen.
Inducción de la Respuesta Inmune en el GALT Organizado
Una vez captados, los antígenos llegan a las células presentadoras de antígeno (APC) en la cúpula subepitelial de las Placas de Peyer o en los ganglios mesentéricos. Las APC procesan los antígenos y presentan péptidos a los linfocitos T vírgenes. Este encuentro, junto con señales coestimuladoras y el ambiente de citocinas, determina el destino de los linfocitos T.
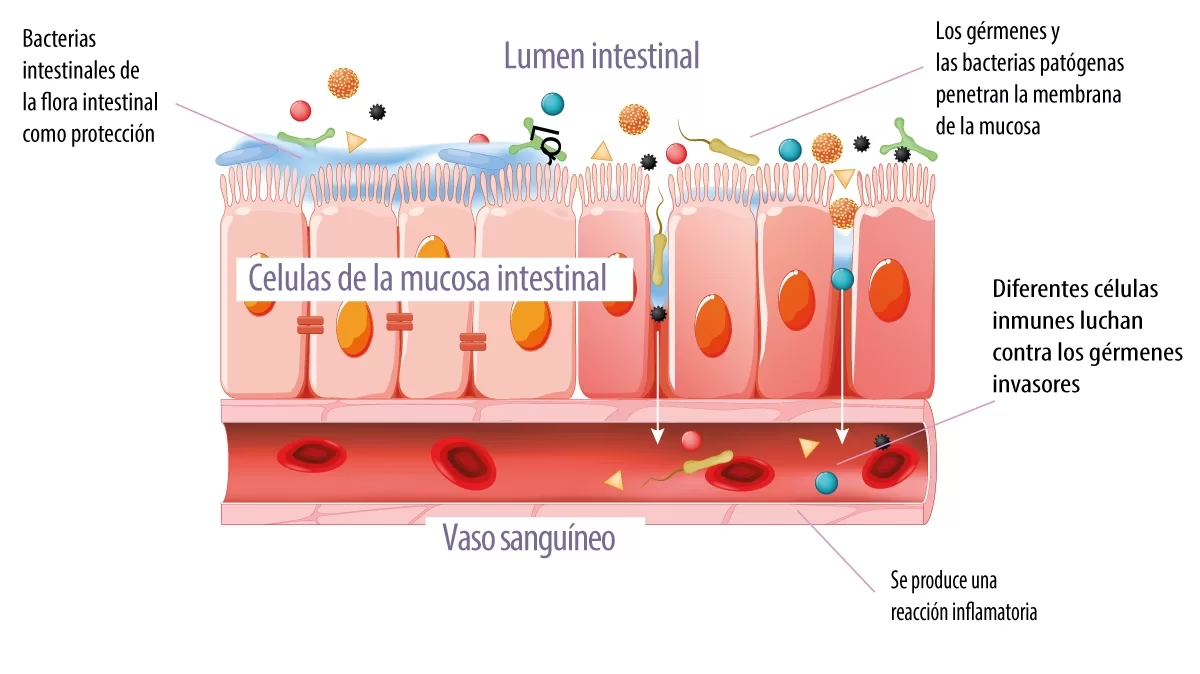
Los linfocitos T colaboradores (Th) vírgenes pueden diferenciarse en varias subpoblaciones efectoras, cada una con funciones y perfiles de citocinas distintos:
- Th1: Secretan IFNγ, IL-2. Importantes para la defensa contra patógenos intracelulares (virus, algunas bacterias) mediada por fagocitos.
- Th2: Secretan IL-4, IL-5, IL-13. Clave en la respuesta contra helmintos y artrópodos, y mediadores de reacciones alérgicas.
- Th17: Secretan IL-17, IL-6. Implicados en la defensa contra bacterias y hongos extracelulares.
- Linfocitos T Reguladores (Tr1, Th3): Secretan IL-10 y/o TGF-β. Cruciales en el intestino para regular la respuesta inmune, prevenir la inflamación excesiva y, fundamentalmente, inducir la tolerancia oral frente a antígenos inocuos de la dieta y la microbiota.
El tipo de citocinas presentes durante la presentación antigénica es determinante para la diferenciación de Th1 (inducida por IL-12), Th2 (IL-4), Th17 (IL-23) y T reguladores (IL-10, TGF-β).
Paralelamente, las citocinas como IL-4, IL-5 y TGF-β también influyen en los linfocitos B en los folículos de las Placas de Peyer, induciendo su diferenciación final a células plasmáticas secretoras de IgA. Estos linfocitos B activados migran a los ganglios mesentéricos para madurar y expandirse, y luego circulan para dirigirse a los tejidos efectores, particularmente la lámina propia intestinal.
Los Anticuerpos Mucosales: IgA, la Estrella Defensiva
La defensa más característica y abundante en las mucosas, y especialmente en el intestino, es mediada por anticuerpos. El isotipo dominante es la IgA secretora (IgA-S), que constituye el 80-90% de las inmunoglobulinas en la mucosa intestinal.
La IgA se sintetiza principalmente en la lámina propia por células plasmáticas diferenciadas a partir de linfocitos B activados en el GALT organizado. La IgA se secreta en forma polimérica (pIgA), generalmente como dímeros unidos por una cadena J. Para ser transportada al lumen intestinal a través de las células epiteliales, la pIgA se une a un receptor específico llamado receptor de Ig poliméricas (pIgR) en la membrana basolateral del enterocito. Este complejo es internalizado y transportado en vesículas hasta la membrana apical, donde es liberado al lumen. Durante este proceso, una parte del pIgR (el componente secretor) queda unido a la IgA, protegiéndola de las enzimas proteolíticas presentes en el lumen intestinal.
La IgA-S tiene funciones cruciales:
- Exclusión Inmune: Forma inmunocomplejos con antígenos (patógenos, toxinas, componentes de la dieta) en el lumen, impidiendo su adhesión al epitelio y facilitando su eliminación en las heces.
- Neutralización: Puede neutralizar toxinas bacterianas y virus en el lumen.
- No Inflamatoria: A diferencia de otros isotipos como la IgG, la IgA-S no activa potentemente el sistema del complemento ni desencadena respuestas inflamatorias significativas en el lumen, lo cual es ideal para un ambiente con alta carga antigénica como el intestino.
La IgM también se encuentra en la superficie intestinal (6-18%), transportada también por el pIgR, pero es menos abundante y más susceptible a la degradación que la IgA. La IgG, aunque minoritaria en el lumen, puede estar presente por difusión o aumentada en deficiencias de IgA.
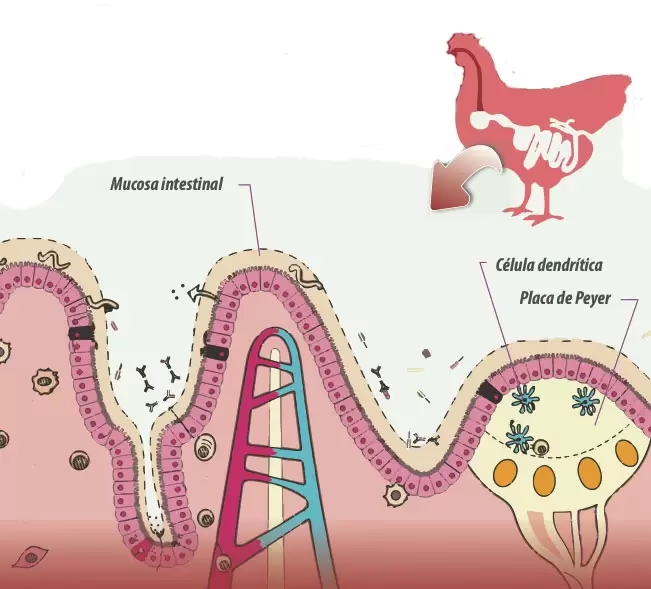
Características Únicas del GALT Moldeadas por la Microbiota
El GALT se distingue de otros tejidos linfoides periféricos (como los ganglios de la piel) por varias razones, muchas de ellas vinculadas a su interacción constante con la microbiota:
- Activación Crónica: La presencia continua de la microbiota mantiene el GALT en un estado de activación basal. Esto se manifiesta en la presencia constante de centros germinales en las Placas de Peyer, incluso en ausencia de infección aguda, a diferencia de los ganglios periféricos que suelen estar quiescentes.
- Antígenos T-Independientes: Muchos componentes de la microbiota, como los polisacáridos capsulares, son antígenos T-independientes. Intriguemente, las IgA producidas contra estos antígenos en el GALT a menudo muestran mutaciones somáticas elevadas y afinidad madura, procesos típicamente asociados con respuestas T-dependientes en centros germinales. Esto sugiere mecanismos únicos en el GALT donde los linfocitos B que reconocen antígenos T-independientes pueden acceder y madurar en centros germinales preexistentes, impulsados por la alta carga antigénica.
- Composición Celular Distintiva: La presencia de poblaciones celulares especializadas como las células M y subpoblaciones únicas de células dendríticas (LysoDCs) y linfocitos T (ciertos IELs) subraya la adaptación del GALT a su entorno.
- Desarrollo de Células B Sistémicas: En algunas especies, incluyendo los humanos, el GALT contribuye al desarrollo de ciertas poblaciones de linfocitos B sistémicos, como las células B de la zona marginal (MZB). Estas células, que residen predominantemente en el bazo, son cruciales para respuestas rápidas a antígenos T-independientes (como los de ciertas bacterias) y pueden adquirir especificidad para antígenos de la microbiota durante su maduración en el GALT.
Tabla Comparativa: Componentes del GALT
| Componente | Ubicación Principal | Función Principal | Células Clave |
|---|---|---|---|
| GALT Organizado | Placas de Peyer, Ganglios Linfáticos Mesentéricos | Inducción de la respuesta inmunitaria | Células M, Células Dendríticas, Linfocitos T y B vírgenes |
| GALT Difuso | Linfocitos Intraepiteliales (IEL), Linfocitos de Lámina Propia (LPL) | Efector de la respuesta inmunitaria, Tolerancia | Linfocitos T (Citotóxicos, Colaboradores, Reguladores), Células Plasmáticas productoras de IgA |
Preguntas Frecuentes sobre el GALT
¿Qué significa la sigla GALT?
Significa Gut-Associated Lymphoid Tissue, que se traduce como Tejido Linfoide Asociado al Intestino.
¿Dónde se localiza el GALT?
Se encuentra disperso a lo largo de todo el tracto gastrointestinal, desde el esófago hasta el recto, pero es más prominente en estructuras organizadas como las Placas de Peyer en el intestino delgado y los ganglios linfáticos mesentéricos.
¿Cuál es la función primordial del GALT?
Su función principal es monitorear el ambiente intestinal para distinguir entre patógenos dañinos y antígenos inocuos (de alimentos o microbiota), montando una respuesta inmune activa contra los primeros e induciendo tolerancia hacia los segundos. También es crucial para la producción de anticuerpos mucosales, especialmente IgA.
¿Cómo logra el GALT tolerar los alimentos y la microbiota?
Mediante mecanismos activos como la inducción de linfocitos T reguladores y la producción de citocinas inmunosupresoras (IL-10, TGF-β), así como la producción de IgA no inflamatoria que confina los antígenos al lumen intestinal.
¿Qué papel tienen las Placas de Peyer?
Son estructuras clave dentro del GALT organizado especializadas en la captación de antígenos del lumen intestinal a través de células M y células dendríticas, e iniciar la respuesta inmune adaptativa.

¿Por qué es tan importante la IgA en el intestino?
La IgA secretora es el anticuerpo más abundante en las mucosas. Actúa principalmente en el lumen intestinal, formando complejos con antígenos para evitar su entrada al organismo. Es resistente a la degradación y no desencadena respuestas inflamatorias agresivas, lo que la hace ideal para la defensa mucosal.
¿La microbiota intestinal afecta al GALT?
Sí, la microbiota es fundamental para el desarrollo y funcionamiento normal del GALT. Mantiene el GALT en un estado de activación crónica, influye en la diferenciación de células inmunes y contribuye a la inducción de tolerancia.
¿El GALT solo protege el intestino?
Aunque su acción principal es local, el GALT puede influir en la inmunidad en otras mucosas (sistema inmune de mucosas compartido) y, en especies como los humanos, contribuye al desarrollo de poblaciones de células B con funciones sistémicas.
Conclusión
El GALT es un pilar fundamental de nuestro sistema inmunitario. Su intrincada estructura y compleja red celular le permiten realizar la tarea vital de proteger nuestro vasto tracto intestinal de las amenazas, mientras mantiene una coexistencia pacífica con los billones de microorganismos que nos habitan y los nutrientes que nos sostienen. Desde la captación especializada de antígenos por las células M, pasando por la orquestación de respuestas celulares y la producción masiva de IgA, hasta su rol en la tolerancia oral y su sorprendente influencia en la inmunidad sistémica a través de células como las MZB, el GALT es un ejemplo maestro de cómo el sistema inmune se adapta a un entorno único y desafiante. Comprender su función es clave para entender la salud digestiva y su conexión innegable con el bienestar general del organismo.
Si quieres conocer otros artículos parecidos a El GALT: Guardián Inmune del Intestino puedes visitar la categoría Acupuntura.

Conoce mas Tipos